本文是一篇医学论文,在我们的调查病例中,女性患者甲状腺微小癌发病率明显超过男性(1VS2.1),这或许是由于雌激素受体α通过促进甲状腺癌细胞的自噬而促进了甲状腺癌的生长,在肿瘤的较早阶段,细胞自噬是一种抑制机制,它消除致癌蛋白底物、受损的细胞器以及有毒的未折叠蛋白,以抑制肿瘤的发展。
资料与方法
1研究对象
2020年1月至2021年1月,在济宁市第一人民医院接受甲状腺切除的PTMC患者,所有参与者都签订知情同意将他们的临床记录用于这项研究。纳入标准为:(1)无放射史及其他头颈部恶性肿瘤患者;(2)行甲状腺切除术和PCND的患者;(3)经手术标本组织病理学检查证实的PTMC;(4)患者电子病历资料完整。排除标准:(1)合并桥本氏病、非PTC(滤泡型、髓质型和间变性)和其他器官转移癌的患者;(2)既往有甲状腺或甲状旁腺手术史的患者;(3)术前有CLNM临床证据的患者;(4)病历资料不完整的患者。180名PTMC患者被纳入了这项研究。本研究得到济宁市第一人民医院伦理委员会的批准。
2研究方法
2.1数据收集
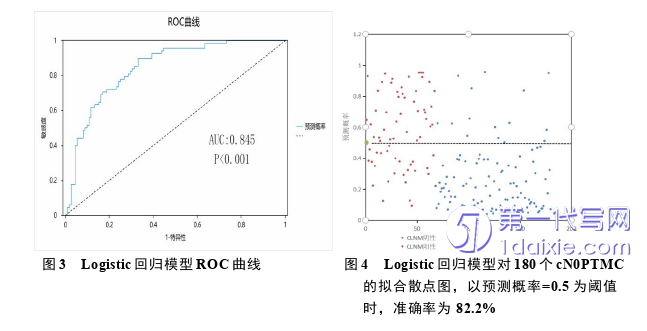
收集了有关cN0 PTMC患者的临床资料、超声检查图像特征、BRAF V600E基因型的数据。所有行pC LD的cN0 PTMC患者,原发病灶和周围引流淋巴结将在手术前通过超声、计算机断层扫描(CT)或细针穿刺活检进行评估,超声和CT检查均未发现淋巴结转移。对怀疑或已经细针穿刺确诊为单侧的PTMC病人进行单侧腺叶切除手术+同侧pC LD;对怀疑或已经细针穿刺确诊为双侧PTMC或峡部PTMC患者进行全甲状腺切除手术+双侧pCLD。采用配备7-12 MHz线性高分辨率探头的迈瑞DC-8EXP超声诊断仪和美国LOGIQ E20超声诊断仪,所有患者的术前甲状腺及引流部位淋巴结超声检查均由具有5年以上甲状腺超声成像经验的医生进行,根据肿瘤直径、多灶性、肿瘤位置、内部微钙化状态、侵润邻近包膜状态和纵横比记录患者的超声特征。如果存在多个可疑恶性超声特征的结节,则直径最大或可疑恶性特征最多的结节为目标甲状腺结节。多灶性原发性病变被定义为甲状腺内的两个或多个癌症部位,根据其在甲状腺是位置又分为双侧多灶和单侧多灶,单个甲状腺内原发性病变(单灶)仅代表甲状腺内的一个肿瘤。根据术前患者甲状腺超声检查或手术记录发现的肿瘤位置,将肿瘤位置分别记为上1/3、中1/3、下1/3和峡部,当优势病灶占据两个相邻部分时,肿瘤的位置由包含超过三分之二的肿瘤体积的部分确定。微钙化概念为钙化点直径<0.1 cm,后方不伴声影也无彗星尾征,此外,当结节内既含有粗钙化又含有微钙化时也记为微钙化[28]。原发性肿瘤的甲状腺外侵犯包括肉眼的甲状腺外侵润和显微镜下的甲状腺外侵润。纵横比≥1是指在超声检查甲状腺时横断面上测量结节的前后径长度超过左右径的长度,否则为纵横比<1。
结果
1 cN0 PTMC患者CLNM的影响因素
180例行pC LD的cN0型PTMC患者,男性58例,女性122例,年龄范围18-69岁,队列按病理标本中中心颈淋巴结转移状态分为两组:CLNM阳性组(68例)和CLNM阴性组(112例)。CLNM阳性组中年龄平均为(42.43±10.47)岁,CLNM阴性组中年龄平均为(47.87±9.19)岁。肿瘤最大直径范围0.2-1.0cm,平均为(0.57±0.24)cm,CLNM阳性组中最大直径平均为(0.64±0.24)cm,CLNM阴性组中最大直径平均为(0.53±0.23)cm。血清TSH浓度范围0.01-9.00μIU/ml,平均(2.50±1.56)μIU/ml,CLNM阳性组中平均浓度为(2.98±1.86)μIU/ml,CLNM阴性组中平均浓度为(2.21±1.27)μIU/ml。血清TPOAb浓度范围0.10-1081.00 IU/ml,平均(39.235±153.46)IU/ml,CLNM阳性组中平均浓度为(35.78±157.17)IU/ml,CLNM阴性组中平均浓度为(41.37±151.81)IU/ml。血清TGAb浓度范围0.00-998.00 IU/ml,平均(26.165±125.67)IU/ml,CLNM阳性组中平均浓度为(25.65±133.96)IU/ml,CLNM阴性组中平均浓度为(26.48±120.98)IU/ml。CLNM阳性组中,男性、女性各占比:44.1%、55.9%,BRAF V600E基因野生型、突变型各占比16.18%、83.82%,单灶、单侧多灶、双侧多灶各占比33.82%、26.47%、39.71%,甲状腺被膜未侵及、侵及各占比32.35%、67.65%,肿瘤位置上、中、下、峡部各占比8.82%、30.88%、47.06%、13.24%,肿瘤纵横比<1、≥1各占比60.29%、39.71%,肿瘤内部未见钙化、见微钙化各占比36.76%、63.24%。CLNM阴性患者中,男性、女性各占比:25.0%、75.0%,BRAF V600E基因野生型、突变型各占比41.96%、58.04%,单灶、单侧多灶、双侧多灶各占比57.14%、30.36%、12.50%,甲状腺被膜未侵及、侵及各占比55.36%、44.64%,肿瘤位置上、中、下、峡部各占比18.75%、38.39%、35.71%、7.14%,肿瘤纵横比<1、≥1各占比51.79%、48.21%,肿瘤内部无微钙化、可见微钙化各占比58.04%、41.96%。
2单因素分析结果(见表1)
CLNM的主要危险因素:年龄(P<0.001)、肿瘤最大径(P=0.006)、血清TSH浓度(P=0.004)、性别(P=0.008)、BRAF V600E基因类型(P<0.001)、多性灶(P<0.001)、甲状腺被膜是否侵润(P=0.003)、肿瘤内部微钙化(P=0.006)。而血清TPOAb浓度(P=0.814)、血清TGAb浓度(P=0.966)、肿瘤纵横比是否≥1(P=0.266)、肿瘤位置(P=0.091)与CLNM差异性不显著。
结果................................13
1 cN0 PTMC患者CLNM的影响因素......................13
2单因素分析结果(见表1).....................13
3 Logistic回归分析结果(见表2).....................13
讨论..............................16
结论...................................25
讨论
纳入这项研究的病人在术前并未表现出CLNM的直接证据,但是在病理中却出现了37.8%的CLNM,单因素和多因素数据分析结果都表明肿瘤最大径≥0.5cm、年龄<45岁、BRAF V600E基因突变型、血清TSH浓度≥2.252μIU/ml和双侧多灶均为诊断cN0 PTMC患者CLNM的独立危险因子。由于血流信号和肿瘤边界状态评估依赖于操作者,受设备调节及人为主观因素的影响较大,本研究未纳入血流信号和肿瘤边界状态。
在我们的调查病例中,女性患者甲状腺微小癌发病率明显超过男性(1VS2.1),这或许是由于雌激素受体α通过促进甲状腺癌细胞的自噬而促进了甲状腺癌的生长,在肿瘤的较早阶段,细胞自噬是一种抑制机制,它消除致癌蛋白底物、受损的细胞器以及有毒的未折叠蛋白,以抑制肿瘤的发展。当肿瘤已经形成时,自噬又促进了肿瘤的生长,可能机制是通过加速细胞内循环程序维持肿瘤存活和促进肿瘤生长,该程序为新陈代谢提供底物,这在肿瘤快速生长阶段可能特别重要,因为快速生长需要持续的营养和能量供给[29],而男性PTMC患者CLNM的发生率(51.7%)明显高于女性(31.1%),一项荟萃分析[30]也认为cN0 PTMC的CLNM频率与男性显著相关(OR 2.33,95%CI1.71-3.17,P=0.003)。男性患者正常较高的基础代谢率可能导致肿瘤细胞过度增殖并导致转移[31],提示男性PTMC患者的初始治疗策略应与女性有所不同。但在本研究中引入年龄、肿瘤直径等因素后男性不是诊断CLNM的独立危险因素。
结论
1.术前血清TPOAb水平、血清TGAb水平、肿瘤位置、纵横比≥1均不是诊断CLNM的独立危险因素,尽管在单因素分析中性别、甲状腺被膜侵润和肿瘤内部微钙化可以有效预测cN0 PTMC患者发生CLNM,但当结合其他因素进行多因素分析时他们都不是cN0PTMC患者发生CLNM的独立危险因素。
2.年龄<45岁是诊断cN0 PTMC患者发生CLNM的独立危险因素,其OR值较大,敏感度、阴性预测值和预测准确率均较高,特异度和阳性预测值相对偏低。
3.肿瘤最大直径≥0.5cm是诊断cN0 PTMC患者发生CLNM的独立危险因素,其OR值较大,敏感度、阴性预测值较高。特异度、阳性预测值和预测准确率最低。
4.术前血清TSH≥2.252μIU/ml是诊断cN0 PTMC患者CLNM的独立危险因素,其OR值较大,敏感度、阴性预测值和预测准确率相对较高,而特异度和阴性预测值相对较低。
5.BRAF V600E基因突变型是诊断cN0 PTMC患者发生CLNM的独立危险因素,其OR值较大,敏感度和阴性预测值最高,预测准确率较低,而特异度和阳性预测值最低,BRAF V600E野生型不是CLNM的独立危险因素。
参考文献(略)
