本文是一篇医学论文范文,笔者经过研究,得出结论:新型冠状病毒SARS-CoV-2辅助蛋白ORF7a通过泛素化修饰,增强其对STAT2磷酸化的抑制能力,从而增强其对宿主I型干扰素信号转导的抑制作用。
第1章 SARS-CoV-2编码蛋白对I型干扰素产生通路的抑制作用
1.1 材料
1.1.1 细胞
HEK293T细胞、A549细胞均购自美国生物标准品资源中心(America Type Culture Collection, ATCC)。HEK293T细胞生长于含10%胎牛血清(Fetal bovine serum, FBS)和1%双抗(青霉素/链霉素)的DMEM培养基中,放置在37 °C、5% CO2的温箱中培养;A549细胞生长于含10% FBS、1%双抗(青霉素/链霉素)、1%非必须氨基酸和1%丙酮酸钠的DMEM培养基中,放置在37 °C、5% CO2的温箱中培养。
1.1.2 质粒构建
分别将SARS-CoV-2编码的所有病毒蛋白所对应的基因克隆至携带CMV启动子的真核表达载体pXJ,并将标签蛋白Flag或EGFP的基因融合在病毒编码蛋白基因的C’端。报告质粒pISRE-luc购自Agilent Technologies公司(Cat: 219089-51, Santa Clara, CA),质控质粒pG L4.74[phRluc/TK(]phRluc-TK)购自Promega公司(Cat: E6921, Madison, WI)。报告基因pIFN-β-luc及干扰素信号通路关键分子[RIG-I (2CARD)、 MAVS、 TBK1、 IKKε和IRF3/5D]的真核表达质粒均由美国德克萨斯大学医学部生物化学与分子生物学系Pei-Yong Shi教授课题组提供。核转运受体蛋白(KPNA1-6)基因克隆自HEK293T细胞总mR NA,扩增的基因片段克隆至真核表达载体pXJ,并将标签蛋白HA的基因融合在核转运受体蛋白基因的C’端。
1.2 方法
1.2.1 SARS-CoV-2编码蛋白的体外表达
将状态良好的HEK293T细胞传代,接种至6孔板(1×106个/孔),37 °C 培养过夜。使用X-treme-GENETM 9转染试剂将0.5-2 μg病毒编码蛋白真核表达质粒瞬时转染至6孔板内的HEK293T细胞。37 °C 继续培养36 h;随后弃去培养基,使用PBS(PH 7.4)清洗细胞2遍,收集细胞,使用IP裂解液在4 °C 旋转裂解1 h。将裂解后样品离心20 min(4 °C、15,000 rpm),将收集得到的上清液进行Werstern blot分析。
1.2.2 IFN-β启动子双荧光素酶报告试验
将状态良好的HEK293T细胞传代,接种至24孔板(1×105个/孔),37 °C 培养过夜。使用X-treme-GENETM 9转染试剂,分别将20-80 ng的SARS-CoV-2编码蛋白真核表达质粒和10 ng携带萤火虫荧光素酶基因的报告质粒pIFN-β-luc及4 ng 携带海肾荧光素酶基因的质控质粒phRluc-TK共转染HEK293T细胞,并设置空质粒对照(保证转染的总质粒量为100 ng)。同时,每个实验组还需共转染通路刺激物[RIG-I (2CARD)、 MAVS、 TBK1、 IKKε或IRF3/5D]的真核表达质粒(4 ng/孔),并设置空质粒刺激物对照。在转染后24 h弃去上清液,使用PBS清洗细胞一次并收集。将收集得到的细胞严格按照说明书进行双荧光素酶活性检测。用各孔测得的萤火虫荧光素酶活性数值比各孔测得的海肾荧光素酶数值以标准化各孔的转染效率,随后将所得数值除以其未加通路刺激物的对照组数值,从而得到I型干扰素通路诱导的倍数。将空质粒pXJ对照组所得数值设置为100%,并将实验组各蛋白的诱导效率与对照组EGFP比较,通过软件进行差异性分析。每次每个实验组及对照组的转染均做3个重复,实验结果求其平均值。
第2章 SARS-CoV-2编码蛋白对I型干扰素信号转导通路的抑制作用
2.1 材料
2.1.1 细胞
HEK293T细胞、Vero细胞均购自美国生物标准品资源中心(America Type Culture Collection, ATCC)。HEK293T细胞、Vero细胞均生长于含10%胎牛血清(Fetal bovine serum, FBS)和1%双抗(青霉素/链霉素)的DMEM培养基中,放置在含37 °C、5% CO2的温箱中培养。
2.1.2 质粒构建
报告质粒pISRE-luc购自Agilent Technologies公司(Cat: 219089-51, Santa Clara, CA),质控质粒pG L4.74[hRluc/TK(]phRluc-TK)购自Promega公司(Cat: E6921, Madison, WI)。干扰素信号转导通路关键分子(STAT1和STAT2)的真核表达质粒均由美国德克萨斯大学医学部生物化学与分子生物学系Pei-Yong Shi教授提供。本章节所用到的其他质粒同上一章节所述。
2.1.3 试剂
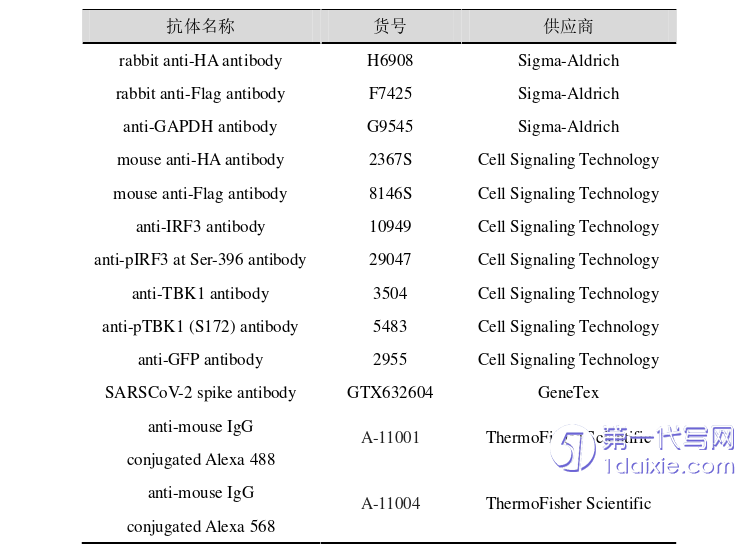
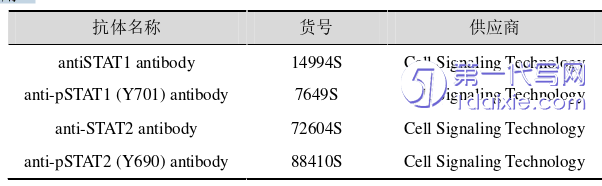
本部分研究所用到的抗体及其他试剂大都同上一章所述,以下抗体为本部分研究所使用:
2.2 方法
2.2.1 ISRE启动子双荧光素酶报告试验
将状态良好的HEK293T细胞传代,接种至24孔板(1×105个/孔),37 °C 培养过夜。使用X-treme-GENETM 9转染试剂,分别将230 ng的SARS-CoV-2编码蛋白真核表达质粒和250 ng携带萤火虫荧光素酶基因的报告质粒pISRE-luc及20 ng 携带海肾荧光素酶基因的质控质粒phRluc-TK共转染HEK293T细胞,并设置空质粒对照(保证转染的总质粒量为500 ng)。在转染后第24 h给予细胞人源IFN-α(1,000 units/mL)处理,放入温箱继续培养细胞8 h。弃去上清液,使用PBS清洗细胞一次并收集。将收集得到的细胞严格按照说明书进行双荧光素酶活性检测。用各孔测得的萤火虫荧光素酶活性数值比各孔测得的海肾荧光素酶数值以标准化各孔的转染效率,随后将所得数值除以其未使用人源IFN-α处理的对照组数值,从而得到I型干扰素通路诱导的倍数。将空质粒pXJ对照组所得数值设置为100%,并将实验组各蛋白的诱导效率与对照组EGFP比较,通过软件进行差异性分析。每次每个实验组及对照组的转染均做3个重复,实验结果求其平均值。
2.2.2 SDS-PAGE及Werstern blot
操作步骤同研究内容第1章1.2.4部分。
2.2.3 间接免疫荧光实验
操作步骤同研究内容第1章1.2.5部分。
第3章 ORF7a泛素化修饰增强其抑制I型干扰素信号转导活性 ............................. 57
3.1 材料 ............................................. 57
3.2 方法 .................................. 58
3.3 结果 ............................................ 60
第4章 高致病性冠状病毒NSP1/6抑制I型干扰素信号转导通路的差异 ................................. 71
4.1 材料 .......................................... 71
4.2 方法 ................................................. 73
4.3 结果 ..................................... 75
结论.......................... 85
第4章 高致病性冠状病毒NSP1/6抑制I型干扰素信号转导通路的差异
由SARS-CoV-2感染引起的COVID-19是一种新出现的可以感染人类和多种动物的、并引起急性呼吸道症状的疾病。目前,COVID-19是一场仍在持续的全球性大流行,严重威胁着全球公共卫生安全,并导致了全球经济的巨大负担。
SARS-CoV-2在病毒分类学上属于冠状病毒科β冠状病毒属,其基因组为一条单股正链RNA,分别编码16个非结构蛋白(NSP1-16)、4个结构蛋白(S、E、M和N)以及若干个辅助蛋白(如ORF3a、ORF3b、ORF6、ORF7a、ORF7b、ORF8及ORF10)。非结构蛋白构成病毒复制酶,调控病毒的复制[207];结构蛋白参与构成病毒粒子并与病毒的侵染过程有关;而辅助蛋白与病毒的复制无关,但具有干扰宿主免疫应答的功能[206, 208]。 SARS-CoV-2反向遗传学系统的建立与发展,使得拯救出具有感染性的活的SARS-CoV-2成为可能,且很大程度上促进了冠状病毒这种具有庞大的基因组的RNA病毒的研究,但是有关活病毒的试验性研究被局限在了生物安全3级(Biosafety level-3, BSL-3)实验室,这严重阻碍了SARS-CoV-2相关研究的发展及相关治疗策略的研究。因此,迫切需要开发一种用于SARS-CoV-2的能摆脱BSL-3束缚的高效试验系统。
本章节研究内容基于SARS-CoV-2反向遗传学系统,通过分子生物学手段将海肾荧光素酶(Renilla luciferase, Rluc)基因插入并替换全基因组第21,563-28,259位核苷酸(包括结构蛋白基因S、M、E及辅助蛋白基因ORF3a、ORF3b、ORF6、ORF7a、ORF7b、ORF8)从而构建SARS-CoV-2复制子系统。随后使用可有效抑制SARS-CoV-2复制的药物瑞德西韦(Remdesivir)验证了该复制子系统的效用。最后将该复制子系统应用于比较不同冠状病毒(SARS-CoV-2、SARS-CoV和MERS-CoV)NSP1和NSP6抑制宿主I型干扰素信号转导活性对病毒复制效率的作用中。
结论
1 新型冠状病毒SARS-CoV-2可通过自身编码的蛋白经由多种途径抑制宿主I型干扰素的产生和信号转导,从而逃逸宿主I型干扰素应答。
2 新型冠状病毒SARS-CoV-2辅助蛋白ORF7a通过泛素化修饰,增强其对STAT2磷酸化的抑制能力,从而增强其对宿主I型干扰素信号转导的抑制作用。
3 新型冠状病毒SARS-CoV-2非结构蛋白NSP1、NSP6具有较高的抑制宿主I型干扰素信号转导的活性,而这可能导致了SARS-CoV-2具有比SARS-CoV和MERS-CoV更强的复制能力。
参考文献(略)
