本文是一篇工程硕士论文,本论文研究了多孔 LiZnPO4 电极材料在强碱性电解液 3 M KOH + 1 wt% LiOH + ZnO + 0.46 M K4P2O7 中的电化学行为,其最高充/放电比容量为 94 mAh·g-1/71 mA h·g-1,SEM 及 EDS 测试表明电极在强碱性电解液浸泡后会形成一层钝化膜,在循环后钝化膜会减弱,电池容量衰减的原因是循环后部分锌溶解进入了电解液,造成电极活性物质的减少。
第一章 绪论
1.1 选题的背景及意义
化石能源枯竭和环境污染是当今世界面临的重大难题[1,2],发展可再生能源日益得到世界各国的重视。二次电池在可再生能源的储存和有效利用,以及缓解化石能源污染环境等方面居于重要地位[3],发展具有理论比能量高、比功率大、资源丰富、环境友好等优点的二次电池已是大势所趋[4]。 目前市场上的二次电池主要有镍氢电池、镉镍电池、铅酸电池、锂离子电池等,但是这些电池都存在的一定的问题。镍氢电池生产成本较高、不耐高温且充电效率较低[5];镉镍电池所用镉元素对环境污染严重[6];铅酸电池体积大,比能量低,充电速度慢,循环寿命短[7,8];锂离子电池由于锂资源有限、成本高和使用有机电解质带来的不安全性限制了其进一步发展[9]。因此,寻找兼具安全、廉价及环保等优势的新型高性能绿色二次电池成为当务之急。
最近几年,以金属锌作为负极材料的二次电池受到人们的关注,如锌镍蓄电池、锌锰二次电池、锌离子电池、锌空气电池等。锌负电极材料主要有以下优点:(1)理论比容量达820 mAh·g-1,是铅的3.2倍;(2)平衡电位低(-0.762 V vs. SHE),析氢过电位大,组成的电池开路电压比较高;(3)在水中的稳定性好;(4)资源丰富,成本低廉,对环境的污染性很小。然而,锌负极由于存在析出枝晶、化学溶解、钝化膜、电位极化较大、析氢等问题,导致锌电池的实际能量密度较低,循环寿命较短,已经成为目前研究的重点。
........................
1.2 锌电池的种类
将锌电池按照其使用的电解液可分为四类:(1)碱性锌电池,该类电池通常采用6 mol·L-1 KOH系水溶液作为电池电解液[13-15];(2)中性锌电池,该类电池常采用Li2SO4、ZnSO4、Na2SO4系水溶液作为电解液[16-18];(3)弱酸性锌电池,该类电池常采用ZnCl2、LiCl、ZnSO4系水溶液作为电解液[19-21];(4)有机电解质锌电池,目前常用的有机电解质包括Zn(CF3SO3)2[22,23]、LiTFSI[24,25]、Zn(TFSI)2[26,27]、聚吡咯(PPy)[28,29],常用的溶剂有乙腈(C2H3N)、碳酸丙烯酯(C4H6O3)、磷酸三乙酯(TEPO)等。
1.2.1 碱性锌电池
碱性锌电池由于具有高工作电压、快速反应动力学和较高的离子电导率等优势而受到广泛使用,如碱性锌银电池[30,31]、碱性锌镍电池[32,33]、碱性锌锰电池[34,35]、碱性锌空电池[36,37]等。碱性锌电池最常用的电解液是 KOH 及 NaOH 水溶液。该类电池具有比能量高、可大电流放电、电池制造成本低、储存期长、耐低温性能好、环境污染小等特点。但碱性锌电池的缺点也很突出,具体表现为锌负极的放电产物锌酸盐等在强碱性电解液中的溶解度较大,锌电极的自腐蚀及枝晶等问题[38,39]导致自放电,造成电池容量衰减。
1.2.2 中性锌电池
中性锌电池与碱性锌电池相比,具有电解液廉价易得、腐蚀性小、可避免电解液碳酸化等优点。虽然其工作电压和放电电流密度不及碱性锌空气电池高,但能满足中、小电流密度放电要求,可在小功率放电场所替代碱性锌电池。Cheng等人[40]研究了 NaCl、KCl、NH4Cl、(NH4)2SO4 等电解质溶液中锌电极和空气电极的电化学行为,结果表明 4 M NH4Cl + 1 M KCl 是一种较好的锌空电池的准中性电解液。Yu 等人[41]考察了 NH4Cl、ZnCl2、KCl 及它们的混合溶液对锌空电池电化学行为的影响,结果表明,低电流密度放电时采用 NH4Cl 作为主体电解质的锌电极性能相对较好,KCl 的加入有利于改善溶液导电性、提高放电电压和延长放电时间,最佳溶液配比为 4 M NH4Cl + 2 M KCl。
..........................
第二章 实验部分
2.1 实验试剂及仪器
本论文中所使用的试剂和设备如表 2-1 和表 2-2 所示。

表 2-1 实验试剂
.............................
2.2 电极的制作
(1)金属锌片电极:将金属锌片表面在金相抛光机上先后用 800 目、1200目、2500 目金相砂纸抛光,除去表面的氧化膜,迅速冲洗干净并放入无水乙醇中保存备用。
(2)锌化合物电极:按 8 : 1 : 1 的质量比分别称取 LiZnPO4 或 ZnO 活性材料、石墨、乙炔黑,并置于研钵中充分研磨 30 min,待混合均匀后加入适量无水乙醇及少量聚四氟乙烯(PTFE,30 wt%)乳液,继续研磨混合至浆料,涂覆于除油后的黄铜网集流体上,面积为 1.0 cm × 1.0 cm,用对辊机辊压至厚度为 0.3 mm,置于 80 ℃的鼓风干燥箱中干燥 8 h,称重并控制活性物质每片极片质量为20 mg 左右。
(3)LiFePO4 电极:采用不锈钢网作为集电极,其他实验步骤同上(2)。
循环伏安测试是控制电极的电位以某一扫描速率从起始电位开始向其他电位方向扫描,到达指定电势后改变扫描的方向,再回扫到某一电位,记录过程中电流与电位的关系,并呈现为循环伏安曲线,该曲线能反应电极在电位窗口内发生的具体氧化还原反应情况,帮助了解电极的电化学反应过程与机理。本论文采用三电极系统在辰华 CHI760E 电化学工作站上进行循环伏安测试,其中辅助电极为碳棒,在低碱性电解液中用 Hg/HgO 电极作为参比电极,在弱碱性、弱酸性电解液中用 Hg/Hg2SO4 作为参比电极,测试电压范围和电位扫描速率随具体实验对象调整。
......................................
第三章 金属锌片电极在非强碱电解液中的电化学行为研究.............................. 17
3.1 金属锌片电极在低碱性电解液中的电化学行为........................... 17
3.1.1 循环伏安与扫描电镜分析........................................ 17
3.1.2 电化学阻抗分析............................................. 18
第四章 LiZnPO4 负极材料的低碱性电解液及电化学行为 .................................. 26
4.1 LiZnPO4 材料的制备与表征 ............................. 26
4.2 低碱性电解液体系的确定......................................... 27
第五章 ZnO 负极的弱碱性电解液及其电化学行为 ................................. 35
5.1 电解液 pH 对 ZnO 电极电化学性能的影响 ............................ 35
5.1.1 pH 对 ZnO 电极循环伏安的影响 .......................................... 35
5.1.2 pH 对 ZnO 电极容量及循环性能的影响 ............................ 36
第六章 弱酸性电解液及 Zn/LiFePO4电池的电化学行为
6.1 弱酸性 Li2SO4-ZnSO4 电解液的确定
6.1.1 电解液中 Li2SO4 及 ZnSO4浓度的确定
为研究电解液中 Li2SO4 的浓度对电池性能的影响,本实验首先分别采用(0.5、1.0、1.5、1.9)M Li2SO4 + 2.4 M ZnSO4 进行测试,电解液 pH 均控制为 4.0。
图 6-1.a 为 Zn/LiFePO4 电池在四种不同 Li2SO4 浓度电解液中的循环容量图。由图可知,电池的放电比容量及循环稳定性随着电解液中 Li2SO4 浓度的增大而增大,在 Li2SO4 浓度为 1.9 M 时首圈放电比容量为 85.6 mAh·g-1,第 100 次放电比容量为 64.6 mAh·g-1,明显高于其他组,故 Li2SO4 浓度采用 1.9 M 为宜。
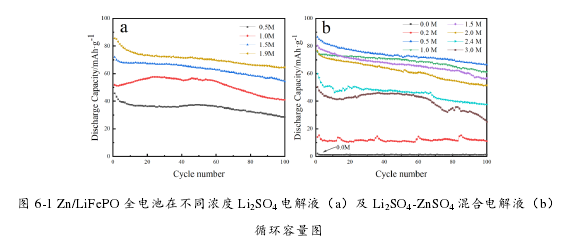
图 6-1 Zn/LiFePO 全电池在不同浓度 Li2SO4 电解液(a)及 Li2SO4-ZnSO4 混合电解液(b)循环容量图
在 Li2SO4 浓度确定为 1.9 M 的基础上,进一步探索了电解液中 ZnS O4 浓度对电池的影响,采用 pH 为 4.0 的 1.9 M Li2SO4 + (0、0.2、0.5、1.0、1.5、2.0、2.4、3.0)M ZnS O4 电解液对电池进行了充放电测试,其充放电容量如图 6-1.b 所示。
由图 6-1.b 可知,当电解液中不加入 ZnSO4 时,电池几乎无容量,表明 ZnSO4的加入是十分必要的。随着电解液中 ZnSO4 浓度的增加,电池的放电比容量先上升后下降,在 0.5 M 时电池的放电比容量最大,首圈放电比容量为 86.8 mAh·g-1,第 100 圈的放电比容量为 66.6 mAh·g-1,明显高于其他组,故 ZnSO4 浓度采用 0.5 M 为宜。
..................................
第七章 结论
金属锌具有比容量高、资源丰富、绿色环保等优势,可作为二次水系锌电池 的良好电极材料。但金属锌及其锌化合物负极材料在水系电解液中表面容易生成对其电化学过程至关重要的钝化膜,该覆盖膜的消长与电解液酸碱度密切相关。本论文研究了不同酸碱度电解液中金属锌的电化学特性及钝化情况,然后采用了三种不同的锌负极材料,分别研究了其在强碱性、弱碱性及弱酸性电解液中的电化学行为,并探索了相应的反应机理。研究结果如下:
(1)采用金属锌作为研究电极,分别研究了其在 3 M KOH 电解液、pH=9.0的 1.0 M Li2SO4 电解液及 pH=5.0 的 1.9 M Li2SO4 电解液中的电化学行为及钝化情况,结果表明,金属锌电极在三种电解液中均存在一定的钝化情况。①在 3 M KOH 电解液中,金属锌电极在氧化过程中产生致密的钝化膜,该钝化膜会极大抑制电极的电流密度,在还原过程中到达-1.08 V 左右电位时该钝化膜会溶解或破裂,导致出现一个反转的氧化电流峰。②在 1.0 M Li2SO4 弱碱性电解中,金属锌电极电位氧化回扫导致表面形成较多沟壑,当继续大电流对电极进行氧化则会导致绒状 ZnO 层附着在电极表面,造成一定程度的钝化。③在 1.9 M Li2SO4 弱酸性电解液中,当氧化电流较大时,表面会形成较薄的一层 ZnO 钝化膜。
(2)研究了多孔 LiZnPO4 电极材料在强碱性电解液 3 M KOH + 1 wt% LiOH + ZnO + 0.46 M K4P2O7 中的电化学行为,其最高充/放电比容量为 94 mAh·g-1/71 mA h·g-1,SEM 及 EDS 测试表明电极在强碱性电解液浸泡后会形成一层钝化膜,在循环后钝化膜会减弱,电池容量衰减的原因是循环后部分锌溶解进入了电解液,造成电极活性物质的减少。
(3)研究了 ZnO 电极在 pH 值为 9.0 的 1.0 M Li2SO4 + 1.2 M Na2SO4 + 1.2 M (NH4)2SO4 + ZnSO4(饱和)电解液中的电化学性能,结果表明,1.2 M (NH4)2SO4的加入能够有效地减弱锌电极在该电极液中的钝化,其最高充放电比容量高达548.2 mAh·g-1/599.1 mAh·g-1,但是该电极容量衰减较快,20 次充放电循环后其容量保持率 49.9%,这可能由于 Zn2+在电解液中的溶解所致,如果能够抑制 Zn2+在该电解液中的溶解,电池有望获得较高的循环容量及容量保持率。
参考文献(略)
